Möguleg tengsl Janssen og blóðtappa
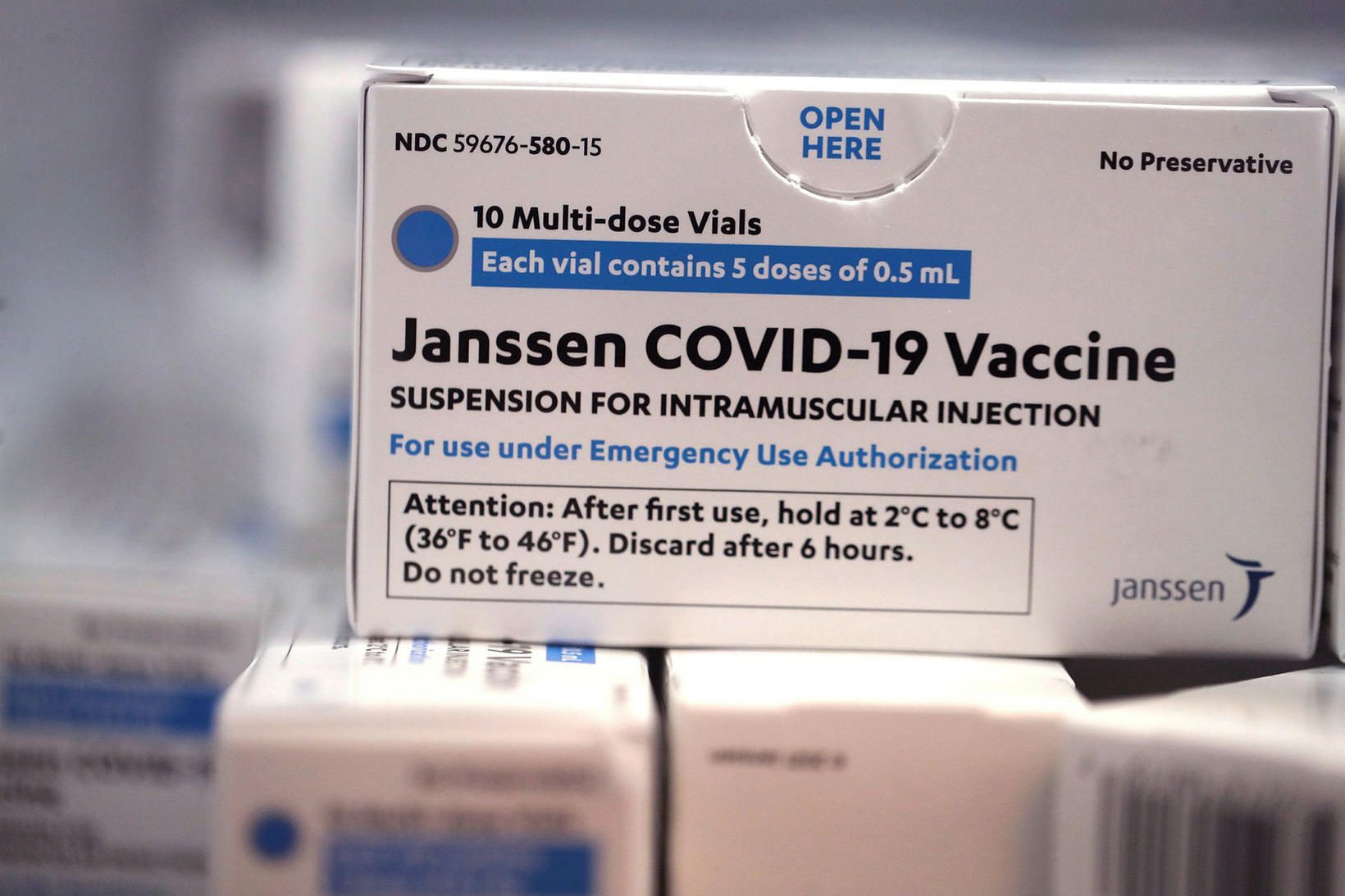
Lyfjastofnun Evrópu (EMA) hefur fundið möguleg tengsl milli bóluefnisins Janssen og mjög sjaldgæfrar tegundar blóðtappa sem urðu til þess að yfirvöld í Evrópu og Bandaríkjunum gerðu hlé á bólusetningum við COVID-19 með bóluefninu í síðustu viku.
Lyfjastofnunin sagði í yfirlýsingu í dag að öryggisnefnd hennar hefði komist að þeirri niðurstöðu að bæta ætti viðvörun við upplýsingar um bóluefnið sem framleitt er af Johnson & Johnson en bætti þó við að ávinningur af bóluefninu væri meiri en áhætta þess.
Lyfjastofnunin rannsakaði átta alvarleg tilfelli blóðtappa, þar af eitt dauðsfall, sem áttu sér stað í Bandaríkjunum, þar sem meira en 7 milljónir hafa verið bólusettir með bóluefninu.
Öll tilfellin komu fram hjá fólki yngri en 60 ára, meirihluti þeirra voru konur, og mynduðust blóðtapparnir innan þriggja vikna frá bólusetningu. Eins og í tilfelli AstraZeneca bóluefnisins birtust flestir blóðtapparnir í heila og kvið. Niðurstaðan var sú að tilfellin „ættu að vera skráð sem mjög sjaldgæfar aukaverkanir“ bóluefnisins.
„Heilbrigðisstarfsmenn og aðrir sem fá bóluefnið ættu að vera meðvitaðir um möguleika á mjög sjaldgæfum tilvikum blóðtappa innan þriggja vikna frá bólusetningu,“ sagði stofnunin.
Tilkynningin kemur í kjölfar þess að framkvæmdastjóri Evrópusambandsins, sem sér um bóluefnabirgðir sambandsins, sagðist vera fullviss um að 27 aðildarríki ESB myndu hafa næga skammta til að bólusetja að fullu 70% fullorðinna íbúa þeirra um miðjan júlí.
Johnson & Johnson stöðvuðu notkun á bóluefni sínu í Evrópu í síðustu viku og ráðlögðu stjórnvöldum að geyma skammtana þar til Lyfjastofnunin hefði gefið út leiðbeiningar um notkun þeirra.



 DeepSeek kemur á óvart: Kínverjar að taka forystu?
DeepSeek kemur á óvart: Kínverjar að taka forystu?
 Ísland á niðurleið í leitarvélum
Ísland á niðurleið í leitarvélum
 Rússar missa mikilvæga höfn
Rússar missa mikilvæga höfn
 Fólk sem „vill koma aftur“ hafi skorað á Guðlaug
Fólk sem „vill koma aftur“ hafi skorað á Guðlaug
 Landsbankinn segir að skoða þurfi málið nánar
Landsbankinn segir að skoða þurfi málið nánar
 Viðræður mættu ganga betur
Viðræður mættu ganga betur