ESB samþykkir bóluefni Pfizer
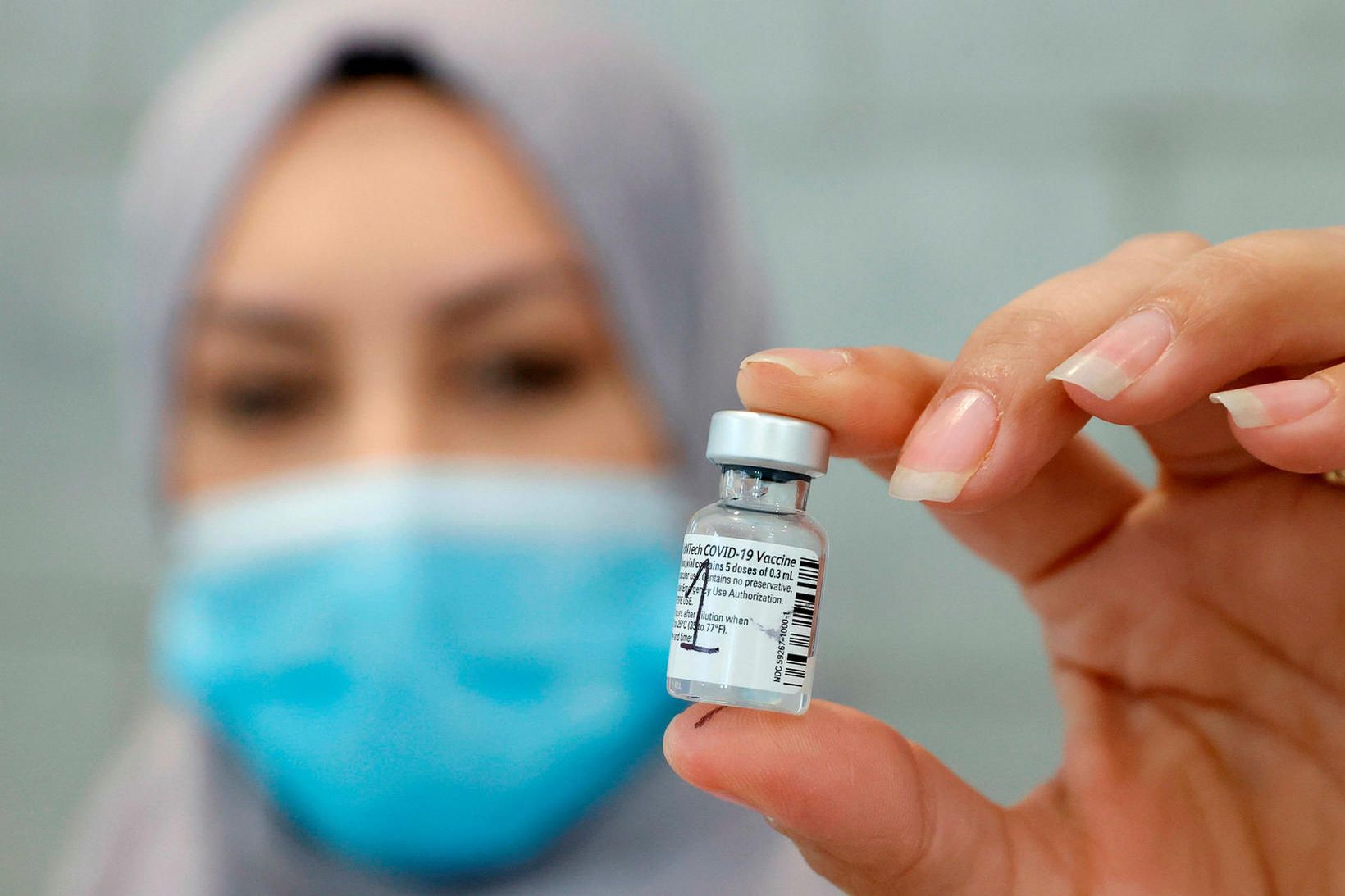
Lyfjastofnun Evrópu hefur veitt markaðsleyfi fyrir bóluefni lyfjafyrirtækjanna Pfizer og BioNTech. Þetta þýðir að bólusetning getur hafist í löndum Evrópusambandsins og á Íslandi innan nokkurra daga.
„Það er mér ánægja að tilkynna að vísindanefnd lyfjastofnunarinnar hittist í dag og mælti með því að markaðsleyfi yrði gefið út í Evrópusambandinu fyrir bóluefnið sem þróað var af Pfizer og BioNTech,“ sagði Emer Cooke, forstjóri stofnunarinnar á blaðamannafundi í dag en niðurstaða nefndarinnar sem tekur fyrir lyf fyrir menn var samhljóða.
Cooke sagði einnig að engar vísbendingar væru á þessari stundu um að bóluefnið virkaði ekki gegn nýju afbrigði veirunnar, sem upp hefur komið í Bretlandi.
Íslensk stjórnvöld hafa í samstarfi við Evrópusambandið tryggt sér kaup á 170.000 skömtum af bóluefninu, sem duga fyrir bólusetningu 85.000 manns. Stefnt er að því að bólusetningar hefjist á milli jóla og nýárs.Svandís Svavarsdóttir heilbrigðisráðherra hefur sagt að um 3.000 skammtar mun berast af bóluefninu í hverri viku frá 27. desember og út mars.
Auk bóluefnisins frá Pfizer/BioNTech hafa íslensk stjórnvöld samið um kaup á 230.000 skömmtum af bóluefni frá sænsk-breska fyrirtækinu Astra Zeneca og Oxford-háskóla og dugar það fyrir 115.000 manns. Þar er prófunum í þriðja fasa lokið en ekki liggur fyrir hvenær þeir koma. Stefnt er að því að hefja afhendingu í Evrópu á fyrsta ársfjórðungi nýs árs.
Yfir 90% virkni
„Tíðindi dagsins eru virkilega ánægjuleg, þar sem baráttan við faraldurinn getur nú hafist af fullum krafti. Nú er að hefjast nýr kafli hjá okkur. Hingað til hafa lyf skipt afar miklu máli í baráttu við kórónuveiruna en bólusetning mun breyta hér öllu. Það er mikilvægt að vel takist til og við höfum úthald í að klára þetta saman,“ er haft eftir Rúnu Hauksdóttur Hvannberg, forstjóra Lyfjastofnunar Íslands, í tilkynningu.
Bretar voru fyrsta þjóðin til að veita lyfinu markaðsleyfi fyrr í þessum mánuði en síðar hafa Kanada, Bandaríkin, Mexíkó og nokkur önnur ríki fylgt í kjölfarið.
Þróun bóluefnisins hófst strax í janúar og hófust tilraunir í apríl. Í nóvember hafði það þegar verið prófað á 40.000 manns og sýndu rannsóknir yfir 90% virkni innan sjö daga frá því seinni skammtur þess er tekin. Algengustu aukaverkanir eru vægir verkir þar sem bóluefnið er tekið, þreyta og hausverkur. Alvarlegar aukaverkanir, á borð við ofnæmisviðbrögð, hafa hins vegar verið mjög sjaldgæfar og engin langtíma eftirköst hafa komið upp.
Fréttin hefur verið uppfærð





 Fer annan hring í borginni og framkvæmdir frestast
Fer annan hring í borginni og framkvæmdir frestast
 „Það þarf einhverja viðhorfsbreytingu“
„Það þarf einhverja viðhorfsbreytingu“
 „Svakalega öflug lægð“
„Svakalega öflug lægð“
 Gætu verið án rafmagns í viku
Gætu verið án rafmagns í viku
 Sviptur leyfi eftir hundamisnotkun
Sviptur leyfi eftir hundamisnotkun
 Stefnan foreldrum „til skammar og minnkunar“
Stefnan foreldrum „til skammar og minnkunar“
 Kennarar hafi ekki svarað foreldrum
Kennarar hafi ekki svarað foreldrum