Tilkynnt um alvarlegar aukaverkanir hjá sex börnum
Tengdar fréttir
Kórónuveiran Covid-19
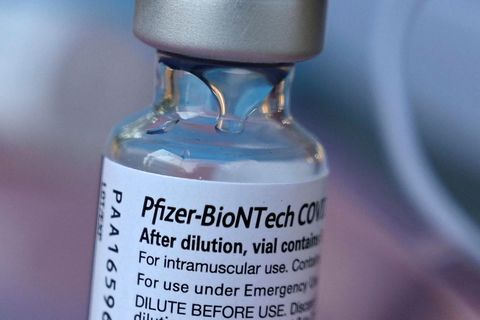
Lyfjastofnun hefur borist sex tilkynningar um alvarlegar aukaverkanir í kjölfar bólusetningar barna á aldrinum 12-17 ára. Þetta kemur fram í svari stofnunarinnar við fyrirspurn mbl.is.
Alvarleg aukaverkun er skilgreind sem svo, að talið sé að notkun lyfs hafi leitt til dauða, lífshættulegs ástands, sjúkrahúsvistar eða lengingar á sjúkrahúsvist, valdið fötlun eða fæðingargalla.
Þrjár tilkynninganna voru vegna sjúkrahúsvistar, en viðkomandi voru ekki í lífshættu. Í hinum þremur tilvikunum reyndist þörf á ítarlegri læknisskoðun og rannsóknum á einkennum.
Ekki með þekktan undirliggjandi sjúkdóm
„Slíkar tilkynningar eru í sumum tilvikum taldar alvarlegar ef sérfræðingar Lyfjastofnunar meta það svo að ómeðhöndluð eða alvarlegri tilfelli hefðu mögulega getað endað t.d. með sjúkrahúsvist,“ segir í svari stofnunarinnar.
Þetta sé í samræmi við leiðbeiningar um lyfjagát, þar sem slíkar tilkynningar séu flokkaðar sem klínískt mikilvægar.
„Þessir sex einstaklingar sem umræddar tilkynningar varða voru ekki með þekktan undirliggjandi sjúkdóm þegar grunur um aukaverkun í kjölfar bólusetningar vaknaði. Í öllum tilvikum nema einu var einstaklingum batnað eða á batavegi þegar tilkynning barst. Ekki hafa borist viðbótarupplýsingar fyrir sjöttu tilkynninguna að svo stöddu.“
Orsakasamhengi ekki staðfest
Tekið er fram að þegar tilkynningar vegna gruns um aukaverkun berast Lyfjastofnun, sé ekki vitað hvort orsakasamhengi sé á milli bólusetningar og tilkynnts atviks.
Tilkynningarnar séu síðan metnar ásamt öllum öðrum tilkynntum tilvikum í samevrópskum lyfjagátargagnagrunni, í samstarfi við aðrar stofnanir á EES-svæðinu og Lyfjastofnun Evrópu.
„Þannig er hægt að meta upplýsingar í hverju tilfelli fyrir sig en einnig skoða samnefnara á milli tilfellanna, en reynist mynstur svipað í tilkynntum tilfellum styður það við mat á orsakasambandi.“
Enn fremur sé ekki hægt að nota tilkynningar á borð við þessar til að reikna út tíðni aukaverkana af lyfjum/bóluefnum, enda séu þær ekki ætlaðar til þess.
„Það er margt sem hefur áhrif á hvort einkenni séu tilkynnt eða ekki. Tíðni aukaverkana er reiknuð út frá gögnum úr klínískum rannsóknum, og eftir markaðssetningu er líka hægt að styðjast við t.d. faraldsfræðilegar rannsóknir.“
Tengdar fréttir
Kórónuveiran Covid-19
Bloggað um fréttina
-
 Inga G Halldórsdóttir:
Það er allt sem styður að börn myndi ónæmi með …
Inga G Halldórsdóttir:
Það er allt sem styður að börn myndi ónæmi með …
-
 Ingólfur Sigurðsson:
Ráðum við sjálf ferðinni eða elítan?
Ingólfur Sigurðsson:
Ráðum við sjálf ferðinni eða elítan?
-
 Geir Ágústsson:
Mjög áríðandi ábending áður en sprauta 2 er sett í …
Geir Ágústsson:
Mjög áríðandi ábending áður en sprauta 2 er sett í …
-
 Jón Magnússon:
Óafsakanlegt ábyrgðarleysi sóttvarnaryfirvalda
Jón Magnússon:
Óafsakanlegt ábyrgðarleysi sóttvarnaryfirvalda
Fleira áhugavert
- Leiddur á brott af lögreglu
- Möguleiki á að sjá deildarmyrkva í dag
- RÚV leiðréttir sig
- Ráðgerir lokað brottfararúrræði
- Baldur: Bandaríkin vilja ráða yfir Íslandi
- #71. - Sykurpabbi kemur út úr skápnum og ráðherrar sakaðir um ósannindi
- Þjófnaður á verkum er óboðlegur
- Jón Gunnar tekur sæti í stjórn rafeyrisfyrirtækis
- Gul viðvörun víða um land á morgun
- Endurskoða ekki innviðagjaldið
- Misbauð hegðun borgarfulltrúa: „Ég biðst afsökunar“
- #71. - Sykurpabbi kemur út úr skápnum og ráðherrar sakaðir um ósannindi
- Erlendir þjófar stela frá gestum á Þingvöllum
- Jón Gnarr tók vakt á Stuðlum í gær
- Framkvæmdir kærðar til lögreglu
- „Þetta var alveg svakalegt“
- Kínverska sendiráðið gagnrýnir íslensku lögregluna
- Leiddur á brott af lögreglu
- Gamalt kónganafn frá Víetnam
- Bókasafn og hjálpartækjaverslun í eina sæng
- Leiddur á brott af lögreglu
- Ásthildur Lóa fékk algjöra sérmeðferð hjá bankanum
- Ásthildur vildi bætur frá ríkinu eftir eigin mistök
- Misbauð hegðun borgarfulltrúa: „Ég biðst afsökunar“
- Leiddist á glapstigu í verkfalli kennara
- Vinsælustu nöfnin 2024
- #71. - Sykurpabbi kemur út úr skápnum og ráðherrar sakaðir um ósannindi
- „Hún var fyrirmyndarnemandi“
- Afsláttur bankans til Ásthildar Lóu skattskyldur
- Forsendur brostnar
Innlent »
Fleira áhugavert
- Leiddur á brott af lögreglu
- Möguleiki á að sjá deildarmyrkva í dag
- RÚV leiðréttir sig
- Ráðgerir lokað brottfararúrræði
- Baldur: Bandaríkin vilja ráða yfir Íslandi
- #71. - Sykurpabbi kemur út úr skápnum og ráðherrar sakaðir um ósannindi
- Þjófnaður á verkum er óboðlegur
- Jón Gunnar tekur sæti í stjórn rafeyrisfyrirtækis
- Gul viðvörun víða um land á morgun
- Endurskoða ekki innviðagjaldið
- Misbauð hegðun borgarfulltrúa: „Ég biðst afsökunar“
- #71. - Sykurpabbi kemur út úr skápnum og ráðherrar sakaðir um ósannindi
- Erlendir þjófar stela frá gestum á Þingvöllum
- Jón Gnarr tók vakt á Stuðlum í gær
- Framkvæmdir kærðar til lögreglu
- „Þetta var alveg svakalegt“
- Kínverska sendiráðið gagnrýnir íslensku lögregluna
- Leiddur á brott af lögreglu
- Gamalt kónganafn frá Víetnam
- Bókasafn og hjálpartækjaverslun í eina sæng
- Leiddur á brott af lögreglu
- Ásthildur Lóa fékk algjöra sérmeðferð hjá bankanum
- Ásthildur vildi bætur frá ríkinu eftir eigin mistök
- Misbauð hegðun borgarfulltrúa: „Ég biðst afsökunar“
- Leiddist á glapstigu í verkfalli kennara
- Vinsælustu nöfnin 2024
- #71. - Sykurpabbi kemur út úr skápnum og ráðherrar sakaðir um ósannindi
- „Hún var fyrirmyndarnemandi“
- Afsláttur bankans til Ásthildar Lóu skattskyldur
- Forsendur brostnar






 Leiddur á brott af lögreglu
Leiddur á brott af lögreglu
 Möguleiki á að sjá deildarmyrkva í dag
Möguleiki á að sjá deildarmyrkva í dag
 Íslendingur í Bangkok: „Við fengum enga viðvörun“
Íslendingur í Bangkok: „Við fengum enga viðvörun“
 Innviðaskuldin ekki öll í fjármálaáætlun
Innviðaskuldin ekki öll í fjármálaáætlun
 Baldur: Bandaríkin vilja ráða yfir Íslandi
Baldur: Bandaríkin vilja ráða yfir Íslandi
 Þarf að auka varnir á norðurslóðum
Þarf að auka varnir á norðurslóðum
 Skortur á lækningabúnaði hamlar aðstoð
Skortur á lækningabúnaði hamlar aðstoð