Bjóða Evrópu 50 milljónir skammta af Spútnik V
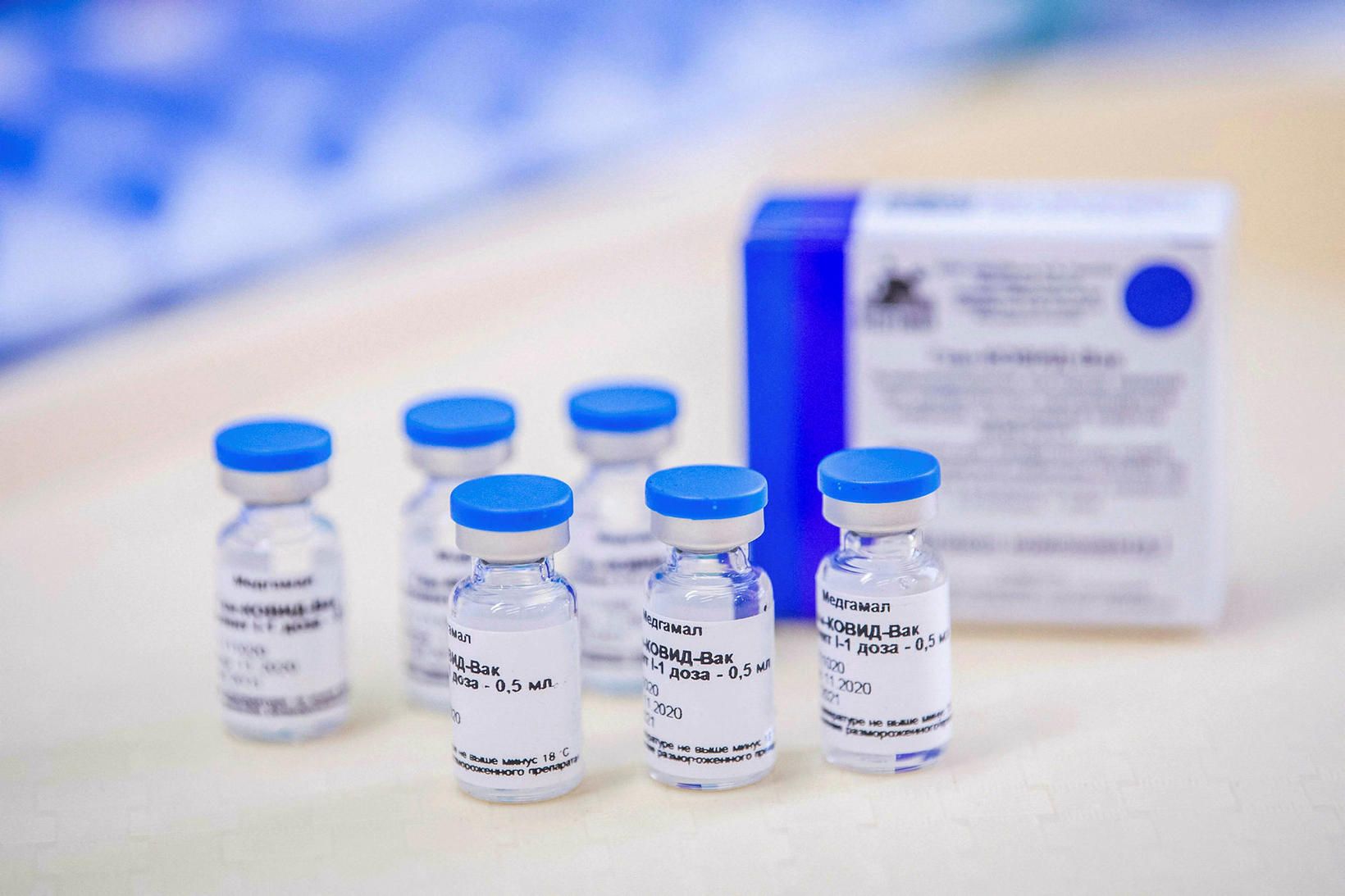
Ef Lyfjastofnun Evrópu veitir Spútnik V-bóluefninu markaðsleyfi í Evrópu geta Rússar boðið upp á bóluefni fyrir 50 milljónir Evrópubúa frá og með júní.
Þetta segir yfirmaður rússneska fjárfestingarsjóðsins, Kirill Dmitriev, sem stendur á bak við Spútnik V-bóluefnið. Lyfjastofnun Evrópu hóf að fara yfir fylgigögn með bóluefninu í dag.
Rússar eiga von á því að nokkur ríki Evrópusambandsins muni samþykkja notkun bóluefnisins strax í þessum mánuði.
Virkni Spútnik V er tæplega 92% samkvæmt niðurstöðum rannsóknar sem birt var í læknaritinu The Lancet í síðasta mánuði. Lyfjastofnun Evrópu hefur þegar veitt bóluefnum Pfizer-BioNTech, Moderna og straZeneca-Oxford leyfi í Evrópu og verið er að fara yfir gögn CureVac og Novavax. Von er á því að bóluefni Jansen J&J fái markaðsleyfi 11. mars en aðeins þarf að sprauta einu sinni með því.
Sérfræðinganefnd Lyfjastofnunar Evrópu (EMA) um lyf fyrir menn (CHMP) hefur hafið áfangamat á COVID-19 bóluefninu Spútnik V (Gam-COVID-Vac), sem hefur verið þróað af stofnuninni „Gamaleya National Centre of Epidemiology and Microbiology” í Rússlandi. Umsækjandi á EES-svæðinu er R-Pharm Germany GmbH.
EMA kemur til með að meta gögn eftir þau sem þau verða tiltæk með tilliti til hvort ávinningur af notkun lyfsins vegi þyngra en áhættan af notkuninni. EMA mun meta bóluefnið út frá evrópskum stöðlum um virkni, öryggi og gæði. Áfangamatið heldur áfram þar til nægjanleg gögn liggja fyrir til að sækja formlega um markaðsleyfi.
Hvernig er búist við að bóluefnið virki?
Bóluefninu er eins og öðrum bóluefnum ætlað að búa líkamann undir að verjast sýkingu af völdum SARS-2-CoV-2 veirunnar. Veiran nýtir sér prótein á yfirborði sínu (gaddaprótein) til að komast inn í frumur líkamans og valda COVID-19 sjúkdómi.
Sputnik V inniheldur tvær gerðir adenóveira, Ad26 og Ad5. Þeim hefur báðum verið breytt á þann veg að þær innihalda genaupplýsingar til að framleiða umrædd gaddaprótein. Adenóveirurnar geta hins vegar hvorki fjölgað sér né valdið sjúkdómi. Adenóveiran Ad26 er í fyrri skammti bólusetningarinnnar en Ad5 í þeim seinni til að auka ónæmissvar af bóluefninu.
Þegar bóluefnið hefur verið gefið fara genaupplýsingarnar úr adenóveirunum inn í frumur líkamans sem hefja framleiðslu á gaddapróteinum. Ónæmiskerfið lítur á þau sem framandi fyrirbæri og hefur varnir með því að framleiða mótefni og T-frumur gegn gaddapróteininu. Sú vörn mun síðar koma að gagni til að verja viðkomandi einstakling gegn sýkingu af völdum SARS-CoV-2 kórónuveirunnar, þar sem ónæmiskerfið kemur til með að þekkja gaddapróteinin, ráðast gegn veirunni, og þar með verja einstaklinginn gegn Covid-19.
EMA getur beitt áfangamati (e. rolling review) til að flýta fyrir matsferli vænlegra lyfja eða bóluefna þegar alvarleg heilsuvá er komin upp. Alla jafna þurfa lyfjafyritæki að senda inn öll gögn um virkni, öryggi og gæði lyfja áður en mat hefst, en í áfangamati eru gögnin metin eftir því sem þau verða tiltæk segir á vef Lyfjastofnunar.



 Fullvissa ferðamenn um að hér sé öruggt
Fullvissa ferðamenn um að hér sé öruggt
 Hentugt gos fyrst gýs á annað borð
Hentugt gos fyrst gýs á annað borð
 Nýtt fangelsi í landi Stóra-Hrauns tilbúið 2028
Nýtt fangelsi í landi Stóra-Hrauns tilbúið 2028
/frimg/1/53/7/1530787.jpg) Flogið á milli ljósaskipta
Flogið á milli ljósaskipta
 Viðræður ekkert þokast frá því á þriðjudag
Viðræður ekkert þokast frá því á þriðjudag
 Litlar líkur á að hraunið nái til mannvirkja
Litlar líkur á að hraunið nái til mannvirkja
/frimg/1/53/8/1530849.jpg) Fatlaður drengur fær ekki þjónustu í verkfalli
Fatlaður drengur fær ekki þjónustu í verkfalli
 Þarf að koma til móts við ólíkar þarfir lækna
Þarf að koma til móts við ólíkar þarfir lækna